Gas Ideal
Según el diagrama de fases, la mayor parte de los elementos químicos y las sustancias pueden existir en tres estados, esto es: sólido, líquido y gaseoso. Y cada uno de nosotros puede muy fácilmente determinar esos estados solo observando el comportamiento cuando nos enfrentamos a una sustancia.
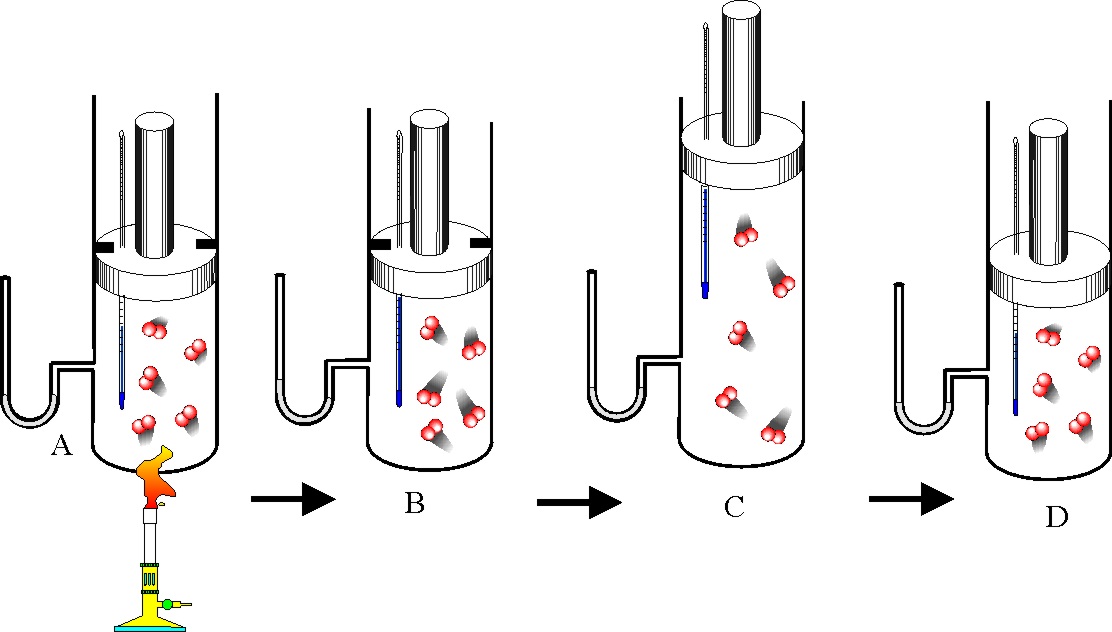
Se define como gas ideal, aquel donde todas las colisiones entre átomos o moléculas son perfectamente elásticas, y en el que no hay fuerzas atractivas intermoleculares. Se puede visualizar como una colección de esferas perfectamente rígidas que chocan unas con otras pero sin interacción entre ellas. En tales gases toda la energía interna está en forma de energía cinética y cualquier cambio en la energía interna va acompañada de un cambio en la temperatura.
Un gas ideal se caracteriza por tres variables de estado: la presión absoluta (P), el volumen (V), y la temperatura absoluta (T). La relación entre ellas se puede deducir de la
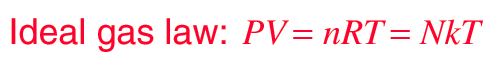
BIBLIOGRAFÍA
- http://www.sabelotodo.org/fluidos/gases.html
- http://hyperphysics.phy-astr.gsu.edu/hbasees/kinetic/idegas.html
No hay comentarios:
Publicar un comentario